Постпункционная гематома бедренной артерии

Эндоваскулярные вмешательства, несмотря на ряд преимуществ перед открытым хирургическим лечением, являются инвазивными методиками и предполагают такие осложнения, как пульсирующие гематомы и ложные аневризмы периферических сосудов, причем их количество увеличивается пропорционально распространению ангиографических методов диагностики и лечения [1, 3–7]. По данным литературы в структуре местных осложнений после пункции артерии ложные аневризмы занимают 60–80% [5]. Для снижения частоты осложнений в настоящее время чаще используют трансаксиллярный, трансбрахиальный и трансрадиальный доступы, ушивающие инструменты. Однако и при таких доступах и развитии эндоваскулярных технологий отмечены повреждения пунктируемой артерии [4–7]. На сегодняшний день актуальными видами лечения пульсирующих гематом и ложных аневризм являются хирургический и компрессионный методы с различными их модификациями [1, 3–5].
Цель работы: проанализировать результаты хирургического и компрессионного методов лечения ложных аневризм и пульсирующих гематом периферических артерий после эндоваскулярных вмешательств.
Материалы и методы исследования
Проанализированы результаты лечения 87 больных с пульсирующими гематомами и ложными аневризмами, находившихся в институте им. Н. В. Склифосовского с 2010 г. по январь 2018 г., в возрасте от 40 до 83 лет. У всех пациентов причиной патологии являлись эндоваскулярные вмешательства, 69 (79,3%) из которых выполнены в других лечебных учреждениях, с последующим поступлением по экстренным показаниям в сроки после манипуляций от 4 суток до 2 месяцев. Большая часть ложных аневризм (23 (88,5%) из 26 случаев) выявлена у пациентов с выполненными эндоваскулярными вмешательствами на коронарных артериях, причем у 14 (53,8%) больных с ложной аневризмой из 23 пациентов было выполнено стентирование коронарных артерий на фоне приема дезагрегантных препаратов (клопидогрел (Плавикс)).
Локализация повреждения: бедренная артерия в 75 случаях (86,2%), подмышечная артерия — 9 (10,3%), плечевая артерия — 2 (2,3%), в одном случае лучевая артерия. Из подтвержденной сопутствующей патологии артериальная гипертензия отмечена у 79 пациентов (90,8%); ожирение II–III степени у 21 (24,1%); сахарный диабет 2 типа средней тяжести у 25 (28,7%); атеросклеротический постинфарктный кардиосклероз у 44 пациентов (50,6%). Атеросклероз артерий нижних конечностей (гемодинамически значимые стенозы/окклюзия поверхностной бедренной артерии) выявлен у 38 больных (43,7%). Прием антикоагулянтных (варфарин, Ксарелто) и дезагрегантных препаратов (клопидогрел (Плавикс, Зилт)) до эндоваскулярных вмешательств отмечен у 61 (70,1%) пациента из 87.
Диагноз ложной аневризмы был установлен 26 (29,9%) больным, пульсирующей гематомы — 61 (70,1%).
При опросе пациентов при поступлении и первичном осмотре обращали внимание на наличие болезненности и припухлости в области выполненной пункции, пульсирующего образования и изменения кожных покровов над ним, систолического шума в области образования. При анализе анамнеза каждого пациента уделяли внимание таким моментам, как давность и объем эндоваскулярного вмешательства; сроки пребывания в стационаре. Ультразвуковое исследование было первым и основным этапом инструментального обследования пациентов. Исследование проведено на ультразвуковой системе Philips iU 22 мультичастотными линейными датчиками L9 — 3 МГц, L15 — 7 МГц.
При выполнении ультразвукового исследования оценивали размеры и количество полостей; длину и диаметр шейки ложной аневризмы (сообщение с сосудом), размер дефекта стенки сосуда, наличие атеросклеротических бляшек в просвете пунктированной артерии (рис. 1).
.png)
.png) При установлении диагноза «ложная аневризма» с целью уточнения локализации поврежденной артерии, подозрения на артериовенозную форму аневризмы, а также решения вопроса о выборе хирургического метода лечения выполняли ангиографию и/или КТ-ангиографию (рис. 2).
При установлении диагноза «ложная аневризма» с целью уточнения локализации поврежденной артерии, подозрения на артериовенозную форму аневризмы, а также решения вопроса о выборе хирургического метода лечения выполняли ангиографию и/или КТ-ангиографию (рис. 2).
Под пульсирующей гематомой понимали пульсирующее опухолевидное образование (до 3,0 см в диаметре) в области пункции с экхимозом и болью в области пункции в сроки от 2–5 суток после вмешательства или ограниченное/диффузное выпячивание сосудистой стенки либо полость, образовавшуюся около стенки сосуда, сообщающуюся с ее просветом в сроки от 2 до 5 суток после манипуляции. Постпункционной ложной аневризмой считали патологическую полость в окружающих тканях, образовавшуюся путем организации околососудистой гематомы вследствие дефекта артериальной стенки и сообщающейся с просветом артерии, в сроки после 17 дней с момента манипуляции.
Результаты исследования
.png) Всем пациентам с пульсирующей гематомой лечение начинали с локальной компрессии давящей повязкой. Дополнительная компрессия системой бедренного сжатия «CompressAR StrongArm tm System» выполнена 14 (22,9%) пациентам из этой группы. Положительным результатом считали тромбоз полости пульсирующей гематомы и отсутствие сообщающегося кровотока с дефектом стенки артерии по данным ультразвукового исследования. Положительный результат получен у 56 (91,8%) больных с пульсирующей гематомой. В первые двое суток проводили попытки локальной компрессии у пациентов с ложными аневризмами. Однако они оказались не эффективны, сопровождались болевым синдромом, пациенты были оперированы (рис. 4).
Всем пациентам с пульсирующей гематомой лечение начинали с локальной компрессии давящей повязкой. Дополнительная компрессия системой бедренного сжатия «CompressAR StrongArm tm System» выполнена 14 (22,9%) пациентам из этой группы. Положительным результатом считали тромбоз полости пульсирующей гематомы и отсутствие сообщающегося кровотока с дефектом стенки артерии по данным ультразвукового исследования. Положительный результат получен у 56 (91,8%) больных с пульсирующей гематомой. В первые двое суток проводили попытки локальной компрессии у пациентов с ложными аневризмами. Однако они оказались не эффективны, сопровождались болевым синдромом, пациенты были оперированы (рис. 4).
Открытое хирургическое лечение выполнено 31 (35,6%) больному, из них 26 пациентов с ложной аневризмой (рис. 5–6) и 5 с пульсирующей гематомой. Сроки выполнения реконструктивной сосудистой операции варьировались от 1 часа до 7 суток. Структура оперативных вмешательств: сосудистый шов артериального дефекта — 28 (90,3%); реконструкция артерии — 3 (9,7%). У всех пациентов удалось добиться восстановления целостности сосуда.
.gif)
.png)
На исход лечения влияли: прием дезагрегантных и антикоагулянтных препаратов и их дозировка до и после эндоваскулярных вмешательств; конституциональные особенности больного, артериальная гипертензия, атеросклеротическое поражение артерии. Положительный исход компрессионного лечения зависел также от величины дефекта артерии, который оценивали по данным ультразвукового метода. При размере дефекта 1–2 мм положительный результат у 46 (92%), при размере 2,1–3 мм — у 4 больных (8%). Эффективность оперативного лечения составила 100%. В послеоперационном периоде был один летальный исход вследствие декомпенсации основного заболевания на фоне до- и интраоперацонной кровопотери; у одного пациента развилась ишемическая гангрена нижней конечности (декомпенсированное кровообращение при поступлении (сахарный диабет)); у трех пациентов отмечалась кожная гиперестезия с последующим регрессом симптоматики через один месяц. Несостоятельности кожных швов, нагноений, лимфорреи, кровотечения из послеоперационной раны не было.
Обсуждение
.png) В настоящее время общероссийские и региональные программы оказания специализированной медицинской помощи ориентированы на повсеместное внедрение эндоваскулярных технологий в диагностический и лечебный процесс сердечно-сосудистых заболеваний [1, 2, 5–7]. Также появляются новые лекарственные средства в антитромботической терапии, разнообразные по механизмам действия и влияющие на все звенья гемостаза [6, 7]. В условиях данной тенденции повышается риск геморрагических осложнений в месте пункции сосуда [1–7]. Несмотря на существующие руководства по методике выполнения эндоваскулярных вмешательств, методы профилактики осложнений, национальные рекомендации, различные ушивающие устройства пациентов с пульсирующими гематомами и ложными аневризмами после эндоваскулярных вмешательств меньше не становится [1, 3–7]. В большинстве научных публикаций не было найдено единого алгоритма по лечению данной патологии при различной локализации на периферических артериях. Также существуют разночтения в сроках формирования ложной аневризмы из пульсирующей гематомы, отсутствие четкого определения термина «ложная аневризма» и «пульсирующая гематома», что зачастую приводит к различному трактованию диагноза и затруднению в правильном выборе тактики и лечения [1]. В данной работе мы попытались проанализировать методы лечения пациентов с данной патологией, определить и систематизировать наиболее подходящую тактику ведения таких больных, выявить оптимальный метод лечения в имеющихся условиях НИИ СП им. Н. В. Склифосовского. На наш взгляд, открытые реконструктивные операции являются оптимальным выбором в лечении ложных аневризм периферических артерий после эндоваскулярных вмешательств, особенно осложненных форм, так как позволяют резецировать саму аневризму с последующим удалением аневризматического мешка и, как следствие, устранить причину сдавления окружающих тканей, в отличие от малоинвазивных методик. Немаловажным является соблюдение мер профилактики после пункционной ангиографии и трансартериальных лечебно-диагностических процедур (давящая повязка, покой конечности, постельный режим и др.), пациентоориентированная беседа с больным до и после манипуляций, которая позволяет значительно уменьшить число постпункционных гематом и последующих ложных аневризм.
В настоящее время общероссийские и региональные программы оказания специализированной медицинской помощи ориентированы на повсеместное внедрение эндоваскулярных технологий в диагностический и лечебный процесс сердечно-сосудистых заболеваний [1, 2, 5–7]. Также появляются новые лекарственные средства в антитромботической терапии, разнообразные по механизмам действия и влияющие на все звенья гемостаза [6, 7]. В условиях данной тенденции повышается риск геморрагических осложнений в месте пункции сосуда [1–7]. Несмотря на существующие руководства по методике выполнения эндоваскулярных вмешательств, методы профилактики осложнений, национальные рекомендации, различные ушивающие устройства пациентов с пульсирующими гематомами и ложными аневризмами после эндоваскулярных вмешательств меньше не становится [1, 3–7]. В большинстве научных публикаций не было найдено единого алгоритма по лечению данной патологии при различной локализации на периферических артериях. Также существуют разночтения в сроках формирования ложной аневризмы из пульсирующей гематомы, отсутствие четкого определения термина «ложная аневризма» и «пульсирующая гематома», что зачастую приводит к различному трактованию диагноза и затруднению в правильном выборе тактики и лечения [1]. В данной работе мы попытались проанализировать методы лечения пациентов с данной патологией, определить и систематизировать наиболее подходящую тактику ведения таких больных, выявить оптимальный метод лечения в имеющихся условиях НИИ СП им. Н. В. Склифосовского. На наш взгляд, открытые реконструктивные операции являются оптимальным выбором в лечении ложных аневризм периферических артерий после эндоваскулярных вмешательств, особенно осложненных форм, так как позволяют резецировать саму аневризму с последующим удалением аневризматического мешка и, как следствие, устранить причину сдавления окружающих тканей, в отличие от малоинвазивных методик. Немаловажным является соблюдение мер профилактики после пункционной ангиографии и трансартериальных лечебно-диагностических процедур (давящая повязка, покой конечности, постельный режим и др.), пациентоориентированная беседа с больным до и после манипуляций, которая позволяет значительно уменьшить число постпункционных гематом и последующих ложных аневризм.
Выводы
- Основным и первым методом лечения пульсирующих гематом является локальная компрессия в течение суток с последующим ультразвуковым контролем.
- На эффективность локальной компрессии влияет прием пациентом антикоагулянтных и дезагрегантных препаратов, конституциональные особенности больного, артериальная гипертензия, локализация и диаметр постпункционного дефекта артерии, комплаентность больного.
- Компрессионное лечение эффективно у больных с пульсирующей гематомой при размере дефекта стенки артерии до 2 мм; при размере дефекта артерии более 2 мм результативно хирургическое лечение.
- Открытое хирургическое лечение эффективно в 100% случаев и является основным методом в лечении ложных аневризм периферических артерий.
Литература
- Гавриленко А. В., Синявин Г. В. Лечение ложных ятрогенных артериальных аневризм // Ангиология и сосудистая хирургия. 2005; 135–138.
- Бочаров С. М. Ангиографическая диагностика и эндоваскулярное лечение при травме артерий. Автореф. дис. … канд. мед. наук. М., 2009. 24 с.
- Seidel A. C., Miranda F. Jr., Fregadolli L. V. Atrogenic pseudoaneurysm of axillary artery // Arg. Bras. Cardiol. 2006; 86 (4): 303–305.
- Houlind K., Jepsen J M., Saicu C. et al. Current management of inguinal false aneurysms//J. Cardiovascular. Surg. 2017; 58 (2): 278–283.
- Панфилов Д. С., Козлов Б. Н., Панфилов С. Д. и др. Проблема лечения постпункционных ложных аневризм: компрессионный, хирургический, пункционный подходы // Сибирский мед. журнал. 2012; 27 (1): 39–44.
- Фокин А. А., Киреев К. А., Москвичева М. Г., Киреева Т. С. Профилактика постпункционных ятрогенных ложных аневризм бедренных артерий после коронарных вмешательств при инфаркте миокарда // Ангиология и сосудистая хирургия. 2016; 22 (2): 139–144.
- Михайлов И. П., Исаев Г. А., Коков Л. С. и др. Использование системного тромболизиса для лечения острой ишемии конечностей // Неотложная медицинская помощь. 2015; 2: 32–34.
Ю. А. Виноградова1
Л. С. Коков, доктор медицинских наук, профессор, член-корреспондент РАН
И. П. Михайлов, доктор медицинских наук, профессор
В. П. Кирющенков
Е. В. Трошкина
ГБУЗ НИИ СП им. Н. В. Склифосовского ДЗМ, Москва
1 Контактная информация: weinstadt235@gmail.com
Методы лечения пульсирующих гематом и ложных аневризм периферических артерий после рентгенэндоваскулярных вмешательств/ Ю. А. Виноградова, Л. С. Коков, И. П. Михайлов, В. П. Кирющенков, Е. В. Трошкина
Для цитирования: Лечащий врач № 7/2018; Номера страниц в выпуске: 21-24
Теги: периферические артерии, осложнения, диагностика, стентирование
Купить номер с этой статьей в pdf
Источник
В статье представлены результаты исследования, посвященного анализу постпункционных ложных аневризмах бедренных артерий и созданию алгоритма тактико-лечебных действий.
Введение
В соответствии с Государственной программой Российской Федерации «Развитие здравоохранения» смертность от ишемической болезни сердца к 2020 г. должна снизиться до уровня 295 на 100 тыс. населения. Для достижения поставленной цели ежегодно будут увеличиваться объемы специализированной медицинской помощи с чрескожными коронарными вмешательствами (ЧКВ), в т. ч. при остром инфаркте миокарда (ОИМ).
Одним из важных условий эффективного проведения эндоваскулярных операций при ОИМ является безопасный артериальный доступ. В соответствии с Клиническими рекомендациями по реваскуляризации миокарда 2018 г. Европейского общества кардиологов и Европейской ассоциации кардиоторакальных хирургов лучевой артериальный доступ (ЛАД) имеет самые высокие уровень и класс доказательности — IА, что делает его эталонным для проведения коронарных интервенций при ОИМ [1–5].
При невозможности интервенций на лучевых артериях применяется бедренный артериальный доступ (БАД), который ассоциирован с большим риском пункционных осложнений по сравнению с ЛАД. Несмотря на правильную технику БАД, ложная аневризма бедренной артерии (ЛАБА) является наиболее частым осложнением в виде массивного кровотечения, особенно на фоне назначения антитромбоцитарных лекарственных препаратов [6].
С учетом наметившихся тенденций, будучи традиционным и классическим, БАД является доступом резерва. Тем не менее БАД всегда будет оставаться востребованным, особенно при необходимости повторных и многократных вмешательств, когда лучевые артерии могут оказаться непригодными для пункций. В сложившихся условиях требуется комплекс мер, направленных на повышение безопасности БАД [7]. Одним из вариантов снижения количества пункционных осложнений является использование специальных устройств для гемостаза. Сравнительная оценка пункционных осложнений при БАД с гемостазом специальными устройствами в сравнении с ЛАД ранее не проводилась, в связи с чем предпринято данное исследование.
Кроме того, несмотря на применение специальных устройств гемостаза, важным условием безопасного проведения БАД является раннее выявление пункционных осложнений и лечебные мероприятия при формировании ЛАБА.
Цель исследования: сравнение пункционных осложнений БАД с гемостазом специальными устройствами и ЛАД в процессе ЧКВ при ОИМ; создание алгоритма тактических и лечебных действий при постпункционных ЛАБА.
Материал и методы
Исследование проведено в НУЗ «Дорожная клиническая больница на ст. Челябинск ОАО «РЖД» по итогам 2014–2016 гг. До 2015 г. БАД использовался рутинно для ургентных ЧКВ, во всех случаях пункционное отверстие в бедренной артерии закрывалось специальными устройствами гемостаза. Начиная с августа 2015 г. внедрен ЛАД. С 2016 г. БАД применялся только у больных с невозможностью использования лучевых артерий (отсутствие пульсации, при шоке, затруднения при заведении ангиографического инструментария).
За период 2014–2016 гг. выполнено 1333 ЧКВ при ОИМ. При анализе историй болезни выделены 2 группы: 1-я группа — применение БАД со специальными устройствами гемостаза — 746 (56,0%); 2-я группа — применение ЛАД — 587 (44%). При БАД использовались следующие специальные устройства гемостаза: ExoSeal (Cordis, США) — 496 (66,5%) и AngioSeal (Terumo, Япония) — 250 (33,5%). Установки устройств гемостаза осуществлялись сертифицированными рентгенэндоваскулярными специалистами, прошедшими специальную подготовку. Устройства гемостаза применялись из имеющихся в наличии в медицинской организации, поэтому сравнительная оценка не проводилась.
Результаты исследования
Частота применения БАД и ЛАД составила в 2014 г. 100% и 0%, в 2015 г. — 66,7% и 36,3%, в 2016 г. — 18% и 82% соответственно. Основным осложнением доступов являлось развитие постпункционных ложных аневризм — 33 (97,1%) из 34 осложнений. В 1 (2,9%) случае зарегистрирована диссекция интимы общей бедренной артерии на фоне С-образной извитости, потребовавшая проведения тромбэндартерэктомии с профундопластикой аутовенозной заплатой. При сравнении ЛАД и БАД зарегистрированы статистически значимые различия (р<0,05) по следующим состояниям: ложная аневризма — 7 (1,2%) и 26 (3,5%) наблюдений (р=0,007); оперированная ложная аневризма — 1 (0,2%) и 8 (1,1%) случаев (р=0,046); общее количество операций с учетом всех местных осложнений — 1 (0,2%) и 9 (1,2%) случаев (р=0,03). У 1 пациента группы БАД проводилась гемотрансфузия. Летальных исходов, связанных с пункционными осложнениями, не зарегистрировано.
Сохраняющаяся потребность в БАД у экстренных пациентов кардиологического профиля обусловила создание алгоритма тактико-лечебных действий при ЛАБА, на который получен патент «Способ выбора тактики лечения больных с подозрением на наличие ятрогенных постпункционных ложных аневризм бедренных артерий» (№ 2641841, заявка от 30.12.2015).
Алгоритм тактико-лечебных действий при ложной аневризме бедренной артерии
На схеме (рис. 1) представлены основные этапы и ключевые тактико-лечебные действия, которые применяются для всех интервенций, выполненных через БАД.
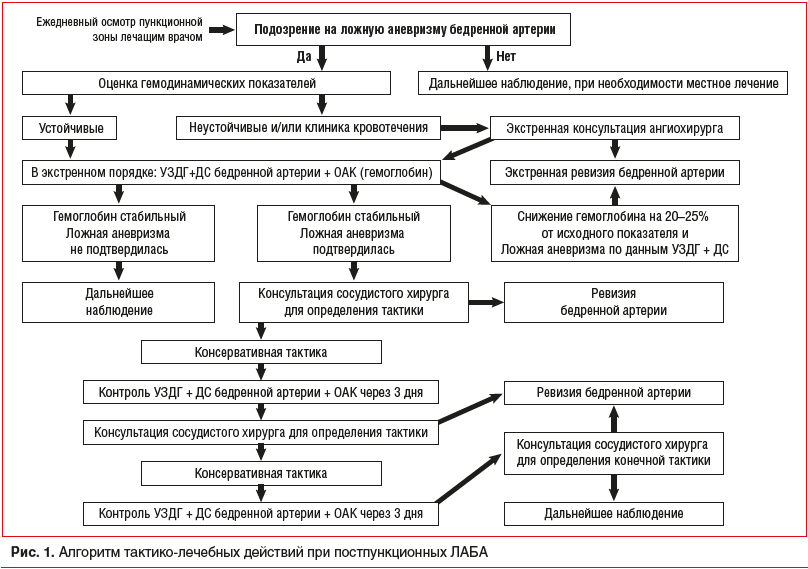
Каждый день оценивается локальный статус зоны бедренной пункции (не менее 2 раз в сутки), включающий жалобы больного, границы подкожной гематомы, наличие образований при пальпации и систолического шума при аускультации. Появление болезненного образования плотной консистенции в проекции бедренной артерии с систолическим шумом над ним позволяет заподозрить ЛАБА. В этой ситуации следующим этапом необходимо провести оценку гемодинамики у больного (артериальное давление, пульс, уровень эритроцитов в крови с гемоглобином).
В рамках данного алгоритма под неустойчивостью гемодинамики понимается снижение артериального давления на 20% и более от значений до вмешательства / привычных показателей и/или снижение гемоглобина на 20% и более от исходного уровня. В обязательном порядке гемодинамические параметры необходимо связывать с основными симптомами возможного кровотечения (ослабление степени наполнения и напряжения пульса, слабость, заторможенность, бледность).
При подозрении на ЛАБА и неустойчивости гемодинамики пациенту проводится дуплексное сканирование (ДС) пункционной зоны и вызывается на консультацию
хирург/ангиохирург, который должен принять решение о дальнейших действиях. При невозможности провести ультразвуковую диагностику и сохранении признаков ЛАБА и кровотечения показана экстренная ревизия.
С учетом данных дуплексного сканирования пункционной зоны и комплексной гемодинамической оценки можно выделить 3 возможных направления для тактико-лечебных действий.
В случаях, когда ЛАБА не выявляется, необходим дальнейший мониторинг за местом доступа.
При отсутствии ЛАБА при ультразвуковой диагностике и неустойчивости гемодинамики решение о ревизии или консервативной тактике принимается индивидуально с обязательным учетом проводимого антитромбоцитарного лечения и общего состояния.
В клинических ситуациях, когда ЛАБА подтверждается, но отсутствуют признаки кровотечения, принимается решение о консервативной тактике: соблюдение строгого постельного режима; компрессия места пункции посредством давящей повязки, которая накладывается заново при ослаблении; отмена антикоагулянтов; из антиагрегантов продолжается прием только блокаторов P2Y12 тромбоцитарных рецепторов (тикагрелор, прасугрел, клопидогрел). Ежедневно пациент консультируется хирургом/ангиохирургом. После 3 дней лечения повторяется дуплексное сканирование пункционной зоны с динамической оценкой псевдоаневризмы. В соответствии с алгоритмом консервативная тактика может проводиться до 6 дней (2 цикла по 3 дня). Если дефект бедренной артерии сохраняется, показано его ушивание.
В обязательном порядке всем больным с феморальными псевдоаневризмами, терапия которых была проведена консервативно, для амбулаторного этапа даются рекомендации, связанные со щадящим режимом (ограничение физических нагрузок) и самостоятельным наблюдением за местом пункции.
Обсуждение
С учетом приоритетной роли эндоваскулярного метода в лечении окклюзионно-стенотической патологии коронарных артерий при ОИМ количество пациентов, нуждающихся в рентгенохирургических вмешательствах, будет увеличиваться. В сложившихся условиях перед рентгенэндоваскулярными специалистами встает задача по обеспечению безопасного и эффективного лечебно-диагностического процесса у больных как с патологией коронарных артерий, так и с проблемами в других артериальных бассейнах.
На современном этапе развития технологий предъявляются серьезные требования к безопасности артериальных доступов для коронарных интервенций при ОИМ. При острой коронарной патологии пациенты уязвимы в отношении пункционных кровотечений. Также у них серьезно ограничены адаптационные механизмы, лежащие в основе способности перенести открытую операцию по ушиванию артериального дефекта в условиях интубационного наркоза.
Зачастую развитие осложнений, ассоциированных с доступом, наблюдается у пациентов старшей возрастной группы с полиморбидностью, и данное обстоятельство серьезно повышает вероятность неблагоприятного исхода.
Понятие эффективности артериального доступа складывается из нескольких составляющих. При ОИМ все манипуляции должны быть четкими и оперативными с учетом дефицита времени. Поэтому врач по рентгенэндоваскулярным диагностике и лечению должен максимально быстро обеспечивать артериальную пункцию и проводить катетеризацию коронарных артерий. Другим важным критерием эффективности является возможность повторного использования данного доступа, особенно это касается пункции лучевой артерии [8].
Несмотря на все положительные возможности ЛАД, отказаться от пункций и катетеризаций бедренных артерий не получится. Как показало исследование, БАД с гемостазом специальными устройствами достоверно (р<0,05) уступил ЛАД по количеству значимых пункционных осложнений. Поэтому важным элементом повседневной клинической практики может стать четкий алгоритм наблюдения за больными с БАД и конкретных регламентированных действий при подозрении и выявлении наиболее часто встречающегося осложнения — ЛАБА.
Выводы
ЧКВ при ОИМ путем лучевого доступа в сравнении с бедренным доступом и рутинным применением специальных устройств гемостаза характеризуется достоверно более низкой частотой (р<0,05) пункционных ложных аневризм (как их общим количеством, так и количеством подвергнутых хирургическому лечению).
Несмотря на рутинное применение ЛАД для ЧКВ при ОИМ, в 2016 г. его доля составила 82,0%, остальные случаи пришлись на БАД.
Сохраняющаяся потребность в использовании БАД обусловливает наличие четкого алгоритма раннего выявления и своевременного лечения основного осложнения — постпункционной ЛАБА, составившей 96,3% от всех осложнений.
Источник
