Гематома бедренной артерии после стентирования

Ангиопластика
Стентирование коронарной артерии — это установка стента (специального каркасного поддерживающего устройства) в суженый атеросклерозом и/или закрытый тромбом участок коронарной артерии.
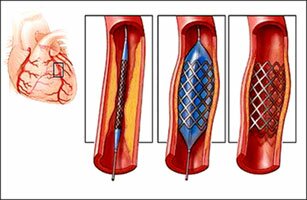
Операция стентирование коронарных артерий производится после выполнения рентгенологического исследования сосудов сердца (коронарографии). Операция начинается также как и при коронарографии, то есть под местной анестезией делается прокол в артерии, куда вводится закрепленный на баллонном катетере стент, и под контролем рентгеновского аппарата подводится к месту сужения сосуда. Достигнув намеченного места, баллон раздувается и вдавливает стент в стенку сосуда, удерживая достигнутое при раздувании баллона увеличение просвета артерии. В зависимости от ситуации может потребоваться не один, а несколько стентов.

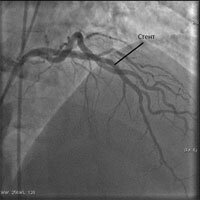
правая коронарная артерия – кровоток перекрыт тромбом, у пациента 2 часовой инфаркт миокарда.
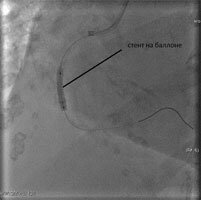
Через закрытый тромбами участок проводится специальный инструмент- проводник, и по нему заводится стент на баллоне. Баллон раздувается, вжимая стент в стенки сосуда, затем все инструменты удаляются, а стент остается поддерживать открытый просвет сосуда.
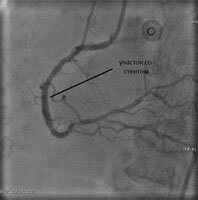
Всегда по завершению операции проверяется правильность установки стента – контрольная ангиография. Затем весь инструмент удаляется, место прокола артерии ушивается и должно оставаться обездвижиным как минимум 12часов.
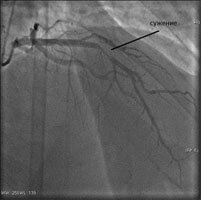
А также при значимых стенозах в артерии.
часто задаваемые вопросы:
1. Сколько времени продолжается стентирование?
Это зависит от сложности проведения стента в нужное место, то есть от анатомии строения сосуда, что бывает очень индивидуально. В среднем, 45 минут — час.
2. Как долго продлитсяреабилитация после стентирования?
Ограничения в режиме после стентирования заканчиваются на следующие сутки — после заживления места пункции (прокола) бедренной артерии. Огромное преимущество внутрисосудистых методов нормализации кровоснабжения сердечной мышцы состоит в том, что они не только не требуют никакой реабилитации.
В течение первых 3-х недель после имплантации стента желательно отказаться от приема алкоголя, стрессовых нагрузок и контрастных воздействий типа сауны и холодных купаний. Кроме того, необходим прием особого препарата (плавикса или брилинты) в течение года после стентирования для профилактики тромбоза стента. Это время необходимо, чтобы стент покрылся внутренней выстилкой сосуда (эндотелий) и не воспринимался организмом как чужеродный материал. Прием этих препаратов увеличивает время свертываемости крови, по этому желательно ограничить травмоопасные виды спорта и воздержаться от плановых операций.
3. Возможно ли повторное сужение в месте установки стента?
Иногда происходит повторное сужение (рестеноз) после стентирования. Связано это с местной реакцией сосуда на стент, тяжестью исходного поражения сосуда, сопутствующими заболеваниями (например, сахарный диабет), а также зависит и от вида установленного стента. Частота рецидивов, в зависимости от перечисленных обстоятельств, может составлять 4-30%. В настоящее время все большей популярностью пользуются стенты с лекарственным покрытием, которые снижают риск развития рестеноза до минимума. Клинитчески заподозрить рестеноз можно при возврате загрудинных болей в первые месяцы после стентирования. В такой ситуации необходимо обратиться к врачу, скорее всего будет назначено исследование функции сердца под нагрузкой (Стресс ЭХО КГ) и повторная коронарография, которые поставит корректный диагноз. Есть методика постановки в стентированый участок нового стента, обязательно с лекарственным покрытием, либо оперативном лечении – аорто-коронарном шунтировании.
Наличие язвы желудка — это риск развития кровотечения. Прием препаратов (плавикса или брилинты и пр.) в течение года после стентирования необходим для профилактики тромбоза стента, они увеличивают время кровотечения, таким образом может открыться кровотечение, остановить которое крайне тяжело, а отменять препараты опасно закрытием стентов и развитием инфаркта миокарда, и чтобы всего этого избежать язву в желудке или 12перстной кишке, кровоточащие геморроидальные узлы и пр. необходимо залечить.
Место прокола выбирается оперирующим врачом, и каждый вариант места прокола артерии имеет свои преимущества и недостатки. Как правило, прокол делают на ноге (в паху). Этот способ наиболее удобен для врача и безопасен для пациента. При поражении артерий ног или брюшной аорты, работать этим доступом сложнее, а порой и вовсе невозможно. Минус такого подхода в том, что после операции коронарографии больному придется лежать, не сгибая ноги, в течение нескольких часов.
Прокол через руку позволяет больному ходить после операции, но такой доступ сложнее для хирурга и более болезненный и рискованный и для пациента. При проколе и введении катетера может развиться спазм артерии руки или тромбоз.
6. Можно ли делать стентирование при инфаркте миокарда?
Можно и нужно это выполнить как можно раньше, не позже первых 6 часов (до развития необратимых изменений в миокарде)от момента развития инфаркта, оптимально — до 2-3 часов. Восстановление кровотока в закрытой артерии в этом временном промежутке резко уменьшает площадь погибшей сердечной мышцы, а иногда позволяет «оборвать» его ход и предотвратить. Нередко стентирование в остром периоде спасает жизнь больному инфарктом. Если осуществить стентирование невозможно, то дальнейшей срочности в его применении, как правило, нет. Однако, возвращение стенокардии в любые сроки после инфаркта является показанием для нормализации коронарного кровотока, поэтому необходимо, не затягивая, сделать коронарографию.
7. На какое время ставится стент?
Срок службы стента не ограничен, а как долго он прослужит вашим сосудам зависит от индивидуальных особенностей организма. А дальнейший прогноз после стентирования определяет состояние коронарных сосудов, точность приема антитромбоцитарных средств после стентирования и степень дальнейшего прогрессирования атеросклероза.
8. Буду ли я чувствовать стент и как его увидеть?
Нет, не будете. Внутри сосуда нет нервных окончаний. Стенты видны на УЗИ сердца и коронарографии после операции, запись которой на диске всегда можно попросить у врача.
9. Можно ли при наличии стентов делать магнитно-резонансную томографию?
Чаще всего можно. Большинство современных стентов не обладают способностью к намагничиванию и МРТ-совместимы. Для полной безопасности в инструкции к стенту указывается срок, который следует воздержаться от проведения МРТ (примерно 8 недель, иногда до 6 месяцев). Но необходимо сообщить врачу, проводящему МРТ, о наличии у Вас стентов и времени, прошедшем после стентирования.
10. Может ли стент сместиться внутри сосуда?
Нет, никогда. Его строение таково, что он удерживается на установленном месте неподвижно.
11. Какие осложнения от коронарографии?
Коронарография — это достаточно безопасная процедура, но все-таки несет некоторые риски для здоровья пациента, поэтому назначает ее только врач и только тогда, когда это действительно необходимо.
Самые частые осложнения это – гематома, реже аневризма в области прокола артерии. При лучевом доступе возможен тромбоз артерии (ее закупорка тромбом). Местные невралгии и парестезии. К счастью подобные проблемы успешно лечатся как в условиях стационара так и при амбулаторном ведении пациента. Также возможно развитие аллергической реакции на контрастное вещество или нарушению функции почек, если они страдали до операции. Согласно статистике вероятность развития серьезных осложнений после коронарографии составляет до 2%. Летальные исходы после коронарографии достаточно редки и возникают не чаще 1 раза на каждую 1000 пациентов, развитие инсульта или инфаркта развиваются как 1 случай на 1000-1500 больных.
Коронарография (коронарная ангиография) — виды, показания и противопоказания, подготовка и проведение, возможные осложнения, отзывы и цена процедуры
05 января, 2015
Коронарография представляет собой диагностическую манипуляцию по исследованию просвета сосудов сердца, которые кровоснабжают миокард. Исследование позволяет выяснить степень сужения коронарных сосудов и оценить степень тяжести ишемической болезни сердца. В ходе коронарографии сначала производится заполнение сердечных артерий специальным контрастным веществом (урографином), после чего врач делает серию рентгеновских снимков. Затем по снимкам изучают состояние и степень сужения коронарных сосудов, и принимают решение о необходимости оперативного лечения, например, стентирования или аорто-коронарного шунтирования.
Именно коронарография позволяет определить оптимальный вид лечения ИБС – шунтирование, стентирование или медикаментозная терапия. В ходе коронарографии дополнительно может быть выполнено УЗИ внутренней стенки сосудов, термография, а также определен градиент давления и резерв кровотока.
При правильном выполнении коронарография является безопасной процедурой, дающей осложнения менее, чем в 1% случаев.
Как еще называют коронарографию?
Термин «коронарография» состоит из двух слов – коронар и графия. Где «коронар» является названием сосудов, приносящих кровь непосредственно к сердечной мышце – миокарду. А «графия» – это общее название всех рентгеновских исследований. Таким образом, общий смысл термина «коронарография» – это рентгеновское обследование сосудов сердца. Поэтому такие названия манипуляции, как «коронарография сосудов» или «коронарография сосудов сердца» являются, по сути, рефреном, повторением или переводом смысла термина.
Для обозначения данной диагностической манипуляции часто используют термины ангиокоронарография, короноангиография или коронарная ангиография. читать далее »
как лечить паховую гематому образовавшуюся после коронарографии
Ошибки при КТ-коронарографии и как их избежать
Источник
Эндоваскулярные вмешательства, несмотря на ряд преимуществ перед открытым хирургическим лечением, являются инвазивными методиками и предполагают такие осложнения, как пульсирующие гематомы и ложные аневризмы периферических сосудов, причем их количество увеличивается пропорционально распространению ангиографических методов диагностики и лечения [1, 3–7]. По данным литературы в структуре местных осложнений после пункции артерии ложные аневризмы занимают 60–80% [5]. Для снижения частоты осложнений в настоящее время чаще используют трансаксиллярный, трансбрахиальный и трансрадиальный доступы, ушивающие инструменты. Однако и при таких доступах и развитии эндоваскулярных технологий отмечены повреждения пунктируемой артерии [4–7]. На сегодняшний день актуальными видами лечения пульсирующих гематом и ложных аневризм являются хирургический и компрессионный методы с различными их модификациями [1, 3–5].
Цель работы: проанализировать результаты хирургического и компрессионного методов лечения ложных аневризм и пульсирующих гематом периферических артерий после эндоваскулярных вмешательств.
Материалы и методы исследования
Проанализированы результаты лечения 87 больных с пульсирующими гематомами и ложными аневризмами, находившихся в институте им. Н. В. Склифосовского с 2010 г. по январь 2018 г., в возрасте от 40 до 83 лет. У всех пациентов причиной патологии являлись эндоваскулярные вмешательства, 69 (79,3%) из которых выполнены в других лечебных учреждениях, с последующим поступлением по экстренным показаниям в сроки после манипуляций от 4 суток до 2 месяцев. Большая часть ложных аневризм (23 (88,5%) из 26 случаев) выявлена у пациентов с выполненными эндоваскулярными вмешательствами на коронарных артериях, причем у 14 (53,8%) больных с ложной аневризмой из 23 пациентов было выполнено стентирование коронарных артерий на фоне приема дезагрегантных препаратов (клопидогрел (Плавикс)).
Локализация повреждения: бедренная артерия в 75 случаях (86,2%), подмышечная артерия — 9 (10,3%), плечевая артерия — 2 (2,3%), в одном случае лучевая артерия. Из подтвержденной сопутствующей патологии артериальная гипертензия отмечена у 79 пациентов (90,8%); ожирение II–III степени у 21 (24,1%); сахарный диабет 2 типа средней тяжести у 25 (28,7%); атеросклеротический постинфарктный кардиосклероз у 44 пациентов (50,6%). Атеросклероз артерий нижних конечностей (гемодинамически значимые стенозы/окклюзия поверхностной бедренной артерии) выявлен у 38 больных (43,7%). Прием антикоагулянтных (варфарин, Ксарелто) и дезагрегантных препаратов (клопидогрел (Плавикс, Зилт)) до эндоваскулярных вмешательств отмечен у 61 (70,1%) пациента из 87.
Диагноз ложной аневризмы был установлен 26 (29,9%) больным, пульсирующей гематомы — 61 (70,1%).
При опросе пациентов при поступлении и первичном осмотре обращали внимание на наличие болезненности и припухлости в области выполненной пункции, пульсирующего образования и изменения кожных покровов над ним, систолического шума в области образования. При анализе анамнеза каждого пациента уделяли внимание таким моментам, как давность и объем эндоваскулярного вмешательства; сроки пребывания в стационаре. Ультразвуковое исследование было первым и основным этапом инструментального обследования пациентов. Исследование проведено на ультразвуковой системе Philips iU 22 мультичастотными линейными датчиками L9 — 3 МГц, L15 — 7 МГц.
При выполнении ультразвукового исследования оценивали размеры и количество полостей; длину и диаметр шейки ложной аневризмы (сообщение с сосудом), размер дефекта стенки сосуда, наличие атеросклеротических бляшек в просвете пунктированной артерии (рис. 1).
.png)
.png) При установлении диагноза «ложная аневризма» с целью уточнения локализации поврежденной артерии, подозрения на артериовенозную форму аневризмы, а также решения вопроса о выборе хирургического метода лечения выполняли ангиографию и/или КТ-ангиографию (рис. 2).
При установлении диагноза «ложная аневризма» с целью уточнения локализации поврежденной артерии, подозрения на артериовенозную форму аневризмы, а также решения вопроса о выборе хирургического метода лечения выполняли ангиографию и/или КТ-ангиографию (рис. 2).
Под пульсирующей гематомой понимали пульсирующее опухолевидное образование (до 3,0 см в диаметре) в области пункции с экхимозом и болью в области пункции в сроки от 2–5 суток после вмешательства или ограниченное/диффузное выпячивание сосудистой стенки либо полость, образовавшуюся около стенки сосуда, сообщающуюся с ее просветом в сроки от 2 до 5 суток после манипуляции. Постпункционной ложной аневризмой считали патологическую полость в окружающих тканях, образовавшуюся путем организации околососудистой гематомы вследствие дефекта артериальной стенки и сообщающейся с просветом артерии, в сроки после 17 дней с момента манипуляции.
Результаты исследования
.png) Всем пациентам с пульсирующей гематомой лечение начинали с локальной компрессии давящей повязкой. Дополнительная компрессия системой бедренного сжатия «CompressAR StrongArm tm System» выполнена 14 (22,9%) пациентам из этой группы. Положительным результатом считали тромбоз полости пульсирующей гематомы и отсутствие сообщающегося кровотока с дефектом стенки артерии по данным ультразвукового исследования. Положительный результат получен у 56 (91,8%) больных с пульсирующей гематомой. В первые двое суток проводили попытки локальной компрессии у пациентов с ложными аневризмами. Однако они оказались не эффективны, сопровождались болевым синдромом, пациенты были оперированы (рис. 4).
Всем пациентам с пульсирующей гематомой лечение начинали с локальной компрессии давящей повязкой. Дополнительная компрессия системой бедренного сжатия «CompressAR StrongArm tm System» выполнена 14 (22,9%) пациентам из этой группы. Положительным результатом считали тромбоз полости пульсирующей гематомы и отсутствие сообщающегося кровотока с дефектом стенки артерии по данным ультразвукового исследования. Положительный результат получен у 56 (91,8%) больных с пульсирующей гематомой. В первые двое суток проводили попытки локальной компрессии у пациентов с ложными аневризмами. Однако они оказались не эффективны, сопровождались болевым синдромом, пациенты были оперированы (рис. 4).
Открытое хирургическое лечение выполнено 31 (35,6%) больному, из них 26 пациентов с ложной аневризмой (рис. 5–6) и 5 с пульсирующей гематомой. Сроки выполнения реконструктивной сосудистой операции варьировались от 1 часа до 7 суток. Структура оперативных вмешательств: сосудистый шов артериального дефекта — 28 (90,3%); реконструкция артерии — 3 (9,7%). У всех пациентов удалось добиться восстановления целостности сосуда.
.gif)
.png)
На исход лечения влияли: прием дезагрегантных и антикоагулянтных препаратов и их дозировка до и после эндоваскулярных вмешательств; конституциональные особенности больного, артериальная гипертензия, атеросклеротическое поражение артерии. Положительный исход компрессионного лечения зависел также от величины дефекта артерии, который оценивали по данным ультразвукового метода. При размере дефекта 1–2 мм положительный результат у 46 (92%), при размере 2,1–3 мм — у 4 больных (8%). Эффективность оперативного лечения составила 100%. В послеоперационном периоде был один летальный исход вследствие декомпенсации основного заболевания на фоне до- и интраоперацонной кровопотери; у одного пациента развилась ишемическая гангрена нижней конечности (декомпенсированное кровообращение при поступлении (сахарный диабет)); у трех пациентов отмечалась кожная гиперестезия с последующим регрессом симптоматики через один месяц. Несостоятельности кожных швов, нагноений, лимфорреи, кровотечения из послеоперационной раны не было.
Обсуждение
.png) В настоящее время общероссийские и региональные программы оказания специализированной медицинской помощи ориентированы на повсеместное внедрение эндоваскулярных технологий в диагностический и лечебный процесс сердечно-сосудистых заболеваний [1, 2, 5–7]. Также появляются новые лекарственные средства в антитромботической терапии, разнообразные по механизмам действия и влияющие на все звенья гемостаза [6, 7]. В условиях данной тенденции повышается риск геморрагических осложнений в месте пункции сосуда [1–7]. Несмотря на существующие руководства по методике выполнения эндоваскулярных вмешательств, методы профилактики осложнений, национальные рекомендации, различные ушивающие устройства пациентов с пульсирующими гематомами и ложными аневризмами после эндоваскулярных вмешательств меньше не становится [1, 3–7]. В большинстве научных публикаций не было найдено единого алгоритма по лечению данной патологии при различной локализации на периферических артериях. Также существуют разночтения в сроках формирования ложной аневризмы из пульсирующей гематомы, отсутствие четкого определения термина «ложная аневризма» и «пульсирующая гематома», что зачастую приводит к различному трактованию диагноза и затруднению в правильном выборе тактики и лечения [1]. В данной работе мы попытались проанализировать методы лечения пациентов с данной патологией, определить и систематизировать наиболее подходящую тактику ведения таких больных, выявить оптимальный метод лечения в имеющихся условиях НИИ СП им. Н. В. Склифосовского. На наш взгляд, открытые реконструктивные операции являются оптимальным выбором в лечении ложных аневризм периферических артерий после эндоваскулярных вмешательств, особенно осложненных форм, так как позволяют резецировать саму аневризму с последующим удалением аневризматического мешка и, как следствие, устранить причину сдавления окружающих тканей, в отличие от малоинвазивных методик. Немаловажным является соблюдение мер профилактики после пункционной ангиографии и трансартериальных лечебно-диагностических процедур (давящая повязка, покой конечности, постельный режим и др.), пациентоориентированная беседа с больным до и после манипуляций, которая позволяет значительно уменьшить число постпункционных гематом и последующих ложных аневризм.
В настоящее время общероссийские и региональные программы оказания специализированной медицинской помощи ориентированы на повсеместное внедрение эндоваскулярных технологий в диагностический и лечебный процесс сердечно-сосудистых заболеваний [1, 2, 5–7]. Также появляются новые лекарственные средства в антитромботической терапии, разнообразные по механизмам действия и влияющие на все звенья гемостаза [6, 7]. В условиях данной тенденции повышается риск геморрагических осложнений в месте пункции сосуда [1–7]. Несмотря на существующие руководства по методике выполнения эндоваскулярных вмешательств, методы профилактики осложнений, национальные рекомендации, различные ушивающие устройства пациентов с пульсирующими гематомами и ложными аневризмами после эндоваскулярных вмешательств меньше не становится [1, 3–7]. В большинстве научных публикаций не было найдено единого алгоритма по лечению данной патологии при различной локализации на периферических артериях. Также существуют разночтения в сроках формирования ложной аневризмы из пульсирующей гематомы, отсутствие четкого определения термина «ложная аневризма» и «пульсирующая гематома», что зачастую приводит к различному трактованию диагноза и затруднению в правильном выборе тактики и лечения [1]. В данной работе мы попытались проанализировать методы лечения пациентов с данной патологией, определить и систематизировать наиболее подходящую тактику ведения таких больных, выявить оптимальный метод лечения в имеющихся условиях НИИ СП им. Н. В. Склифосовского. На наш взгляд, открытые реконструктивные операции являются оптимальным выбором в лечении ложных аневризм периферических артерий после эндоваскулярных вмешательств, особенно осложненных форм, так как позволяют резецировать саму аневризму с последующим удалением аневризматического мешка и, как следствие, устранить причину сдавления окружающих тканей, в отличие от малоинвазивных методик. Немаловажным является соблюдение мер профилактики после пункционной ангиографии и трансартериальных лечебно-диагностических процедур (давящая повязка, покой конечности, постельный режим и др.), пациентоориентированная беседа с больным до и после манипуляций, которая позволяет значительно уменьшить число постпункционных гематом и последующих ложных аневризм.
Выводы
- Основным и первым методом лечения пульсирующих гематом является локальная компрессия в течение суток с последующим ультразвуковым контролем.
- На эффективность локальной компрессии влияет прием пациентом антикоагулянтных и дезагрегантных препаратов, конституциональные особенности больного, артериальная гипертензия, локализация и диаметр постпункционного дефекта артерии, комплаентность больного.
- Компрессионное лечение эффективно у больных с пульсирующей гематомой при размере дефекта стенки артерии до 2 мм; при размере дефекта артерии более 2 мм результативно хирургическое лечение.
- Открытое хирургическое лечение эффективно в 100% случаев и является основным методом в лечении ложных аневризм периферических артерий.
Литература
- Гавриленко А. В., Синявин Г. В. Лечение ложных ятрогенных артериальных аневризм // Ангиология и сосудистая хирургия. 2005; 135–138.
- Бочаров С. М. Ангиографическая диагностика и эндоваскулярное лечение при травме артерий. Автореф. дис. … канд. мед. наук. М., 2009. 24 с.
- Seidel A. C., Miranda F. Jr., Fregadolli L. V. Atrogenic pseudoaneurysm of axillary artery // Arg. Bras. Cardiol. 2006; 86 (4): 303–305.
- Houlind K., Jepsen J M., Saicu C. et al. Current management of inguinal false aneurysms//J. Cardiovascular. Surg. 2017; 58 (2): 278–283.
- Панфилов Д. С., Козлов Б. Н., Панфилов С. Д. и др. Проблема лечения постпункционных ложных аневризм: компрессионный, хирургический, пункционный подходы // Сибирский мед. журнал. 2012; 27 (1): 39–44.
- Фокин А. А., Киреев К. А., Москвичева М. Г., Киреева Т. С. Профилактика постпункционных ятрогенных ложных аневризм бедренных артерий после коронарных вмешательств при инфаркте миокарда // Ангиология и сосудистая хирургия. 2016; 22 (2): 139–144.
- Михайлов И. П., Исаев Г. А., Коков Л. С. и др. Использование системного тромболизиса для лечения острой ишемии конечностей // Неотложная медицинская помощь. 2015; 2: 32–34.
Ю. А. Виноградова1
Л. С. Коков, доктор медицинских наук, профессор, член-корреспондент РАН
И. П. Михайлов, доктор медицинских наук, профессор
В. П. Кирющенков
Е. В. Трошкина
ГБУЗ НИИ СП им. Н. В. Склифосовского ДЗМ, Москва
1 Контактная информация: weinstadt235@gmail.com
Методы лечения пульсирующих гематом и ложных аневризм периферических артерий после рентгенэндоваскулярных вмешательств/ Ю. А. Виноградова, Л. С. Коков, И. П. Михайлов, В. П. Кирющенков, Е. В. Трошкина
Для цитирования: Лечащий врач № 7/2018; Номера страниц в выпуске: 21-24
Теги: периферические артерии, осложнения, диагностика, стентирование
Купить номер с этой статьей в pdf
Источник
